
Recommandations d’utilisation de l’erythropoïetine
I. Indications et Posologies
Erythropoïétine bêta (NEORECORMON® ou biosimilaires)
- Traitement de l’anémie symptomatique des patients adultes atteints de tumeurs solides et traités par chimiothérapie.
- Traitement de l’anémie symptomatique des patients atteints de myélome multiple, de lymphome non hodgkinien de bas grade ou de LLC qui ont un déficit relatif en érythropoïétine et sont sous thérapie antitumorale.
Posologie : 450 UI/kg/sem en SC, peut être administré en 1 ou 3 injections.
Erythropoïétine alpha (EPREX® ou biosimilaires)
- Traitement de l’anémie et réduction des besoins transfusionnels chez les patients adultes traités par chimiothérapie pour des tumeurs solides, des lymphomes malins ou des myélomes multiples et à risque de transfusion en raison de leur état général.
Posologie : 450 UI/kg/sem en SC, peut être administré en 1 ou 3 injections.
Darbépoïétine alpha (ARANESP®)
- Traitement de l’anémie symptomatique chez les patients adultes atteints de pathologies malignes non myéloïdes et recevant une chimiothérapie.
Posologie : 6,75 µg/kg/inj en SC toutes les 3 semaines.
ou 2,25 µg/kg/inj en SC une fois par semaine.
II. Tableau d’adaptation des doses
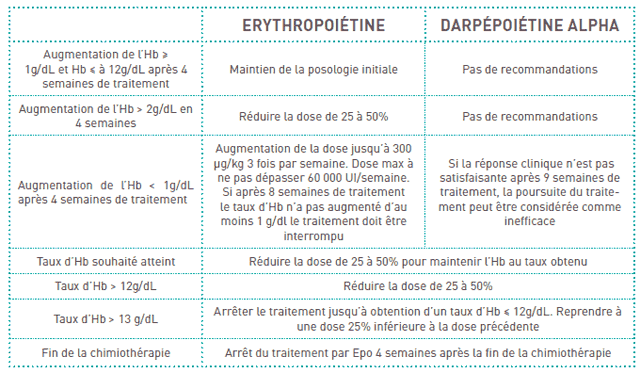
III. Coûts de traitement
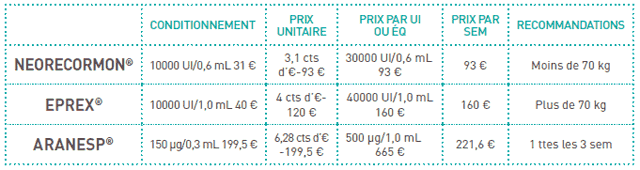
Les prix indiqués dans le tableau sont ceux négociés dans le cadre du marché d’Unicancer. Les prix en ville peuvent être plus élevés.
IV. Rappel des Contre-Indications
Communes à toutes les erythropoïétines
Hypertention artérielle mal contrôlée.
Hypersensibilité connue à la substance active ou l’un des excipients.
Il existe des preuves de niveau I indiquant que les risques d’hypertension artérielle et d’évènements thrombo-emboliques sont légèrement plus élevés chez les patients atteints d’anémie liée à la chimiothérapie et recevant des protéines érythropoïétiques. (Rec. EORTC 2004 et 2006).
V. Statut et Conditions de prescription à l’Gustave Roussy
Médicaments agréés aux collectivités avec A.M.M. et à prescription initiale hospitalière d’une durée de 1 an, renouvellement non restreint
Ordonnance d’initiation pour la phase de correction (1 mois) puis ordonnance d’entretien valable 1 an
Disponibles en pharmacies de ville.
Prescription sur ordonnance nominative
VI. Standards, Options et Recommandations (SOR)
Traitement de l’anémie :
Utilisation de la rHuEPO dans la prise en charge de l’anémie en oncologie médicale et en hématologie
Standards : « Pour un taux d’hémoglobine situé entre 8 et 10 g/dL, en cas de nécessité de correction rapide (moins de 3 semaines), il faut commencer par une compensation par transfusion. Si un traitement carcinologique est en cours ou programmé, un traitement par rHuEPO doit être instauré (niveau de preuve A).
Options : « Pour un taux d’hémoglobine situé entre 10 et 12 g/dL, il est possible de recourir d’emblée à la rHuEPO ou bien d’attendre une chute de ce taux en dessous de 10 g/dL (niveau de preuve B2). Si le taux d’hémoglobine est compris entre 8 et 10 g/dL et qu’aucun traitement carcinologique n’est en cours ou envisagé, un traitement par rHuEPO est possible (hors AMM) dans les tumeurs hématologiques (accord d’experts).
Recommandations : Pas de recommandation
Prévention de l’anémie :
Place de la rHuEPO dans la prévention de l’anémie chez l’adulte
Standards : Pas de standard
Options : Pas d’option
Recommandations : « L’administration de rHuEPO pour la prévention de l’anémie chez l’adulte atteint de cancer n’a de place que dans le cadre d’essais prospectifs randomisés (accord d’experts)
Pré-opératoire :
Place de la rHuEPO en traitement pré-opératoire
Standards : Pas d’attitude standard
Options : « La rHuEPO peut être administrée dans le cadre d’un programme autologue de transfusion en cas de chirurgie carcinologique lourde programmée (accord d’experts).
Recommandations : « L’administration de rHuEPO en pré-opératoire est d’autant plus recommandée qu’il est prévu que la chirurgie soit suivie d’un traitement par chimiothérapie (accord d’experts). L’administration de rHuEPO en traitement pré-opératoire doit être évaluée dans le cadre d’essais prospectifs randomisés d’envergure.
Pour les patients atteints de tumeurs des voies aéro-digestives supérieures, cancer du sein et du poumon à petites cellules. Trois études randomisées de bonne qualité méthodologique et ce en dépit d’une hétérogénéité de recrutement (Henke et al. 2006 et 2003) suggèrent que l’administration d’Epo pourrait avoir un impact délétère (augmentation des risques de décès et de progression loco-régionale), en particulier si le taux d’hémoglobine est > à 12 g/dL.
Il existe des preuves de niveau I (C.BOKEMEYER et al. 2004) indiquant que les risques d’hypertension artérielle et d’évenements thrombo-emboliques sont légèrement plus élevés chez les patients atteints d’anémie liée à la chimiothérapie et recevant un traitement par rHuEPO.
La prescription d’Epo nécessite l’évaluation du bilan martial et éventuellement la prescription d’une supplémentation en fer.
En conséquence, il convient d’être très prudent pour l’utilisation d’Epo en phase adjuvante et néo-adjuvante.
D’autre part, ces traitements engendrent des surcoûts dont l’impact est rapidement visible et signifiant en particulier sur fond de Tarification à l’Activité.
Leur efficacité doit donc être évaluée après 1 mois de traitement et le traitement doit être interrompu devant le constat d’une INEFFICACITE.
Strategie therapeutique (adaptée des sor 2003)
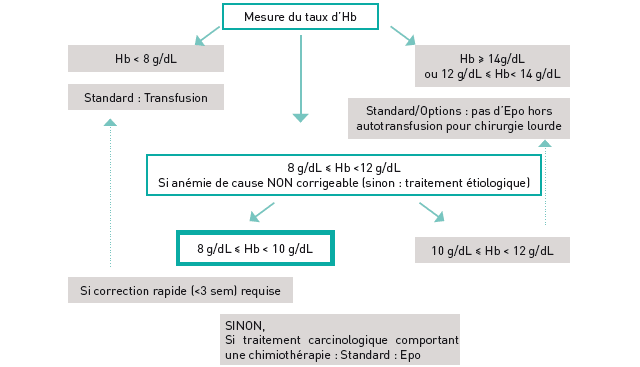
vII. OBJECTIFS MAJEURS
- Concentration cible doit être entre de 12-13 g/dL.
- Amélioration de la qualité de vie des patients.
- Prévention des transfusions
EORTC :
Bokemeyer C et al. European Organisation for Research and Treatment of Cancer (EORTC). Taskforce for the Elderly. EORTC guidelines for the use of erythropoietic proteins in anaemic patients with cancer: 2006 update. Eur J Cancer. 2007 Jan;43(2):258-70. Review.
Aapro MS, Link H. September 2007 update on EORTC guidelines and anemia management with erythropoiesis-stimulating agents. The Oncologist. 2008 13 Suppl 3:33-6.
SOR : Ray-Coquard I et al. Standards, Options et Recommandations (SOR); [Clinical Practice guidelines for the use of erythropoiesis-stimulating agents (ESA: epoetin alfa, epoetin bêta, darbepoetin) in anaemic patients with cancer: 2007 update (summary report)] Bull Cancer. 2008 Apr 1;95(4):433-41. Review. French.
HENKE et al, Do Erytropoietin receptors on cancer cells explain unexpected clinical findings ? ; Journal of clinical Oncology. 2006Oct( 4708-4713).
HENKE et al, Erytropoietin to treat head and neck cancer patients with anaemia undergoing radiotherapy:randomised, double-blind, placebo-controlled trial. Lancet 2003Oct(3621255-60).
Unpublished in peer-reviewed journals. Publicly available in ODAC briefing on US FDA web site.
Bastit L et al. Randomized, multicenter, controlled trial comparing the efficacy and safety of darbepoetin alpha administered every 3 weeks with or without intravenous iron in patients with chemotherapy-induced anemia. J Clin Oncol. 2008 Apr 1;26(10):1611-8.
Pedrazzoli P et al. Randomized trial of intravenous iron supplementation in patients with chemotherapy-related anemia without iron deficiency treated with darbepoetin alpha. J Clin Oncol. 2008 Apr 1;26(10):1619-25.
RCP :Neorecormon® (Roche 2011),Eprex® (JANSSEN-CILAG 2009) et ARANESP® (AMGEN 2011).
F. Netzer, A. Paci, B. Besse, S. De Botton, Médecine, Gustave Roussy
Mise à jour septembre 2012